Nowe podejście w terapii fotodynamicznej nowotworów - fotouczulacze aktywowane in situ
Barbara Lachowicz | 2008-01-11
Leczenie światłem nazywane jest fototerapią, natomiast jeśli światło jest stosowane do wzbudzania uprzednio podanego związku chemicznego nazywa się je fotochemioterapią. Fotochemioterapia liczy sobie ponad 3000 tys. lat. Wykorzystując psoraleny jako fotouczulacze starożytni Indianie oraz Egipcjanie leczyli w ten sposób min. bielactwo. Terapię fotodynamiczną (PDT, photodynamic therapy) powszechnie wykorzystuje się w schorzeniach przednowotworowych i nowotworowych skóry. Polega ona na współdziałaniu światła laserowego oraz fotouczulacza gromadzonego wybiórczo w tkance nowotworowej, w efekcie czego następuje selektywne niszczenie tkanki nowotworowej poprzez aktywację procesów fotobiochemicznych.
Efekt cytotoksyczny i cytoletalny terapii fotodynamicznej wiąże się z wytwarzaniem przez wzbudzony światłem fotouczulacz rodników tlenowych (tlen singletowy, anionorodnik ponadtlenkowy, rodnik wodorotlenowy), które uszkadzają ważne dla życia makromolekuły w komórce, takie jak: białka strukturalne, enzymy, DNA i fosfolipidy. Prowadzi to do śmierci komórek nowotworowych w procesie martwicy lub apoptozy.
Terapia fotodynamiczna wymaga zatem trzech składników:
- barwnika zwanego fotosensybilizatorem, uczulającego tkankę nowotworową na działanie światła,
- źródła światła zdolnego do wzbudzenia zakumulowanego w tkance nowotworowej barwnika,
- tlenu rozpuszczonego w tkance.
Fotouczulacz to związek chemiczny nieulegający przemianom podczas pochłaniania promieniowania. Jako fotouczulacze stosowane są często pochodne kwasu 5-aminolewulinowego (ALA). Kwas ten, będąc produktem przejściowym syntezy hemu, jest naturalnym składnikiem ludzkich komórek. Po aplikacji zewnętrznej substancja ta wnika do guza i wchłaniana jest przez komórki. Włączana jest następnie w cykl przemian komórkowych i prowadzi do akumulacji produktów przemiany kwasu 5-aminolewulinowego, protoporfiryn IX (PpIX). Protoporfiryny po naświetleniu światłem czerwonym (o długości fali 635 nm) stają się naturalnym i endogennym środkiem fotouczulającym, ka[talizatorem reakcji fotochemicznej prowadzącej do śmierci komórki. W tkankach nowotworowych protoporfiryny akumulują się w stężeniach znacznie większych niż w otaczającej ją tkance prawidłowej (po raz pierwszy zjawisko to zaobserwowano w 1924). Natomiast już w latach czterdziestych odkryto, że hematoporfiryna i jej pochodne ulegają selektywnej koncentracji i że są zatrzymywane w tkankach nowotworowych. Środki fotouczulające mogą mieć zastosowanie diagnostyczne lub terapeutyczne. PDT diagnostyczna stosowana jest w celu określenia granicy nowotworu, wyznaczenia miejsca do kontrolnej biopsji, a także monitoringu efektów PDT w trakcie terapii powtarzalnej. Fototerapia terapeutyczna znalazła zastosowanie w onkologii w leczeniu m.in. raka podstawnokomórkowego skóry BCC, raka kolczystokomórkowego skóry SCC i rogowiaka kolczystokomórkowego.
Ogromną zaletą terapii fotodynamicznej jest jej wybiórcze działanie na komórki nowotworowe. Dotychczas efekt ten uzyskiwano przez miejscowe nanoszenie fotouczulacza, jako że jego toksyczne działanie dotyka jedynie te komórki, do których zdoła wniknąć. Autorzy pracy, której wyniki tutaj przytoczę posunęli się o jeszcze jeden krok dalej. Uposażyli mianowicie fotouczulacz w molekularny marker rozpoznawany jedynie w granicach guza i przez to umożliwiający selektywne skierowanie fotouczulacza do jego komórek z krwiobiegu. Co więcej, dzięki dodatkowej właściwości fotouczulacza jaką jest fluorescencja po wzbudzeniu odpowiedniej długości światłem, umożliwili ścisłą kontrolę umiejscowienia i stopnia nasilenia reakcji fotodynamicznej. W rzeczywistości więc, poprzez połączenie stosowanej w diagnostyce nowotworów metody FRET (gdzie sondy fluorescencyjne aktywowane są in situ przez markery nowotworowe) i terapii fotodynamicznej opracowali zupełnie nowe podejście, określone jako koncepcja fotodynamicznych „latarni” molekularnych (PDB - Photodynamic Molecular Bacons).
Skomponowana przez nich cząsteczka określana symbolem PMBMMP7 złożona jest z:
1. fotouczulacza, jakim w tym przypadku jest Pyro,
2. wygaszacza, będącego akceptorem energii wzbudzonego Pyro,
3. peptydu łączącego obie cząsteczki,
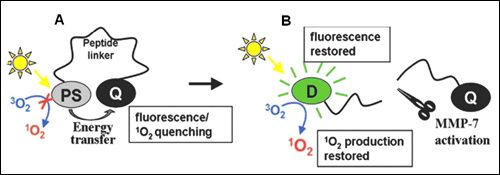
Ryc. 1. Schemat działania PMB (Photodynamic Molecular Bacons).PS – fotouczulacz (ang. photosensitizer), Q – wygaszacz (ang. quencher). [Zheng et al.].
"Pyro" jest to związek z grupy pirofeoforbidów (ang. pyropheophorbids). Po wzbudzeniu światłem czerwonym, przekazuje energię na tlen w stanie tripletowym, generując z dużą wydajnością cząsteczki tlenu singletowego (¬1¬O2). Fluoryzuje przy tym w zakresie bliskiej podczerwieni. Znajdujący się w pobliżu wygaszasz (ang. quencher) BHQ3, pochłaniający fale w zakresie 620-730 nm, przechwytuje energię z Pyro, a przez to uniemożliwia transfer energii na tlen. Sekwencja peptydu łączącego obie cząsteczki (GPLGGLARK) również jest nieprzypadkowa. Oprócz tego, że utrzymuje fotouczulacz i wygaszasz w bliskiej odległości umożliwiając między nimi transfer energii, zawiera również sekwencję rozpoznawaną i rozcinaną przez macierzową metaloproteinazę 7 (MMP7). Właśnie ten enzym został wybrany jako marker nowotworowy, jako że charakteryzuje się wysokim poziomem ekspresji w raku trzustki, jelita grubego, piersi i niedrobnokomórkowym raku płuc.
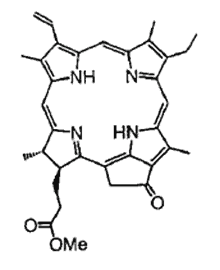
Ryc. 2. Podstawowa budowa cząsteczki związków z grupy pyrofeoforbidów.
Zatem w zamierzeniu eksperymentatorów cząsteczka PMBMMP7 po podaniu do środowiska powinna być specyficznie aktywowana w obrębie komórek nowotworu dzięki produkowanej przez nie MMP7. Uwolniony w ten sposób od wygaszacza fotouczulacz powinien wykazywać aktywność fotodynamiczną pod wpływem promieniowania czerwonego, wnikać do komórek i niszczyć je z udziałem reaktywnych form tlenu. Przy tym widmo emisji fluorescencji powinno wskazywać zarówno miejsce aktywacji, jak i intensywność reakcji fotodynamicznej. Aby sprawdzić, czy założenia pokrywają się z rzeczywistością przeprowadzono testy in vitro.
Testy in vitro
Z wykorzystaniem analizy produktów metodą spektrometrii masowej dowiedziono, że MMP7 aktywuje cząsteczkę PMBMMP7 w roztworze poprzez rozcięcie peptydu łączącego. Cięcia takie nie miało miejsca w przypadku mieszanin PMBMMP7 + MMP2, PMBMMP7 + MMP7 + inhibitor MMP7, jak i mieszaniny MMP7 z cząsteczką PMB zawierającą nierozpoznawaną przez MMP7 sekwencję aminokwasową (PMBnotMMP7).
Natomiast aby udowodnić, że PMBMMP7 może być aktywowana in vitro przeprowadzono testy na liniach komórkowych. Do testów wybrano dwie linie – KB (linia raka jamy nosowo – gardłowej) i BT 20 (linia raka piersi). Pierwsza z nich charakteryzuje się wysokim poziomem ekspresji MMP7 (MMP7+), druga natomiast takiej ekspresji nie wykazuje (MMP7-).
Jak się okazało, silna fluorescencja (a więc aktywacja cząsteczki PMBMMP7) występowała tylko w przypadku komórek KB (MMP7+). Komórki BT 20 (MMP-) charakteryzowało słabe świecenie, porównywalne z uzyskanym w kontroli (jaką była mieszanina MMP7 + PMBnotMMP7). Dowodzi to niezbicie, że tylko pozytywne pod względem syntezy MMP7 komórki są zdolne do aktywacji cząsteczki.

Ryc. 3. Zdjęcia konfokalne komórek linii KB i BT 20 po inkubacji z PMBMMP7 i z PMBnotMMP7. Fluorescencja po lewej i jasne pole po prawej. Barwa czerwona pochodzi od fluoryzującego Pyro. [Zheng et al.]
Dalej należało sprawdzić cytotoksyczność aktywowanego PMBMMP7, a ściślej cząsteczki Pyro. Wykorzystano do tego celu test MTT. Test przeprowadzono w obecności surowicy, ale ponieważ wynik próby, jak i kontroli są podobne, można oczekiwać, że składniki surowicy nie oddziaływują ze składnikami mieszaniny i nie mają wpływu na przeżywalność komórek. Kontrolą były komórki nie traktowane lekiem ani światłem. Wyniki przedstawiają się następująco:
1. Komórki nie traktowane światłem przeżywają nawet w 4 uM stężeniu leku.
2. Obserwuje się znaczny spadek przeżywalności komórek KB będący wypadkową natężenia światła, oraz stężenia leku (zależność podwójnie proporcjonalna).
3. Dawka leku wobec światła o natężeniu 7J/cm2 toksyczna dla komórek KB wynosi 0,5 uM. Komórki BT 20 zachowują pełną żywotność w tych warunkach nawet w obecności leku o stężeniu 4 uM.
Autorzy wykonali również detekcję lokalizacji subkomórkowej Pyro w komórkach KB. W tym celu wykonali barwienia mitochondriów (MitoTracker Green). Zdjęcia ujawniły kolokalizację fluorescencji Pyro i MitoTracker sugerując, że po rozcięciu cząsteczki PMBMMP7 przez matrylizynę 7 Pyro wnika do komórki, gdzie lokuje się w pobliżu mitochondriów. Nie zaobserwowano świecenia w okolicach jądra komórkowego. Ponieważ pożądanym efektem w trakcie terapii fotodynamicznej jest uszkodzenie mitochondriów przez powstające ROS, tendencja Pyro do takiej właśnie lokalizacji czyni z niego skuteczny czynnik destrukcyjny.
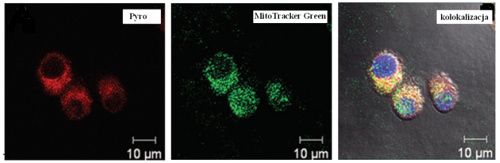
Ryc. 4. Zdjęcia konfokalne ukazujące: lokalizację Pyro (1), MitoTracker Green (2), kolokalizację (3). Na niebiesko jądra komórkowe uwidocznione DAPI. [Zheng et al.].
W celu sprawdzenia czy cytotoksyczność PMBMMP7 wynika z indukcji szlaku apoptotycznego, przeprowadzono barwienie z użyciem Apoptag Plus z fluoresceiną. Zaobserwowano silny sygnał w przypadku komórek traktowanych lekiem i następnie naświetlonych. Wraz z obserwacją o mitochondrialnej lokalizacji Pyro, sugeruje to, iż głównym mechanizmem śmierci komórek jest apoptoza.
Zachęceni wynikami eksperymentu naukowcy podjęli się również oceny aktywności i skuteczności PMBMMP7 in vivo.
Testy in vivo
Wykorzystano dwa osobniki myszy bezgrasiczych, u których zaszczepiono na obu bokach ciała komórki linii KB. PMBMMP7 podano dożylnie jednej z myszy, po czym zaobserwowano u niej silną fluorescencję w obrębie guza. Poddano wówczas oba osobniki naświetlaniu jednostronnemu (30 minut, 135 J/cm2). Już w godzinę później zaobserwowano zapadnięcie się guza naświetlonego guza u myszy potraktowanej PMBMMP7. W ciągu następnych trzech dni zmniejszał się wyraźnie, by po miesiącu zniknąć zupełnie bez oznak nawrotu. W tym czasie nienaświetlony guz u tej samej myszy powiększał się i osiągnął podobne rozmiary, jak guzy u myszy nie traktowanej lekiem.
Metoda proponowana przez autorów pozwala na odejście od koncepcji jak najbardziej selektywnej aplikacji fotouczulacza, bazując raczej na tym, jak selektywny względem komórek nowotworowych jest wybrany marker i jak selektywnie potrafi być zaktywowany zaprojektowany dla niego PMB. Fale inicjujące reakcję fotodynamiczną są z zakresu bliskiej podczerwieni, dzięki czemu mają lepszą zdolność przenikania przez tkankę, co istotne jest zwłaszcza w przypadku guzów głębiej usytuowanych. Proponowany przez grupę Zhenga typ cząsteczki pomaga ulepszyć zarówno obrazowanie, jak i skuteczność terapii. Lecz pokazany tutaj mechanizm separacji fotouczulacza i wygaszacza nie jest jedynym z możliwych. Wysoce prawdopodobne, że podobnie skuteczny mógłby się okazać łącznik np. oligonukleotydowy, z którym hybrydyzowałby specyficzny dla komórek nowotworowych mRNA. Można by też wykorzystać obecność innego enzymu hydrolitycznego, np. specyficznej fosfolipazy.
Nie można autorom zarzucić chyba żadnego błędu metodycznego. Eksperymenty były zawsze opatrzone odpowiednimi kontrolami, także testy in vivo prowadzone były z zachowaniem właściwych prób kontrolnych, w sposób przemyślany i nienarażający niepotrzebnie wysokiej liczby zwierząt na cierpienia. Myszy ponadto hodowane były na diecie niskofluorescencyjnej, dzięki czemu uniknięto artefaktów na obrazie i podniesiono wiarygodność wyników.
Zabrakło być może informacji o wielkości rozwiniętego guza (podano jedynie wielkość pierwotnego inokulum i czas inkubacji - 10E7 komórek, 5 dni), przez co trudno oszacować zdolność PMBMMP7 do penetracji tkanki nowotworowej w funkcji czasu.
Niezbyt trafnym może okazać się również wybór tylko jednej metaloproteinazy. Wiadomo przecież, że profil ekspresji tych enzymów zmienia się w czasie ontogenezy guza. Z drugiej strony komórka nie musi sama ekspresjonować tego enzymu, aby zostać zniszczoną, wystarczy bowiem, że wydzielane przez komórkę sąsiednią lub komórki podścieliska guza enzymy będą „uwalniać” fotouczulacz. Jednakże ma to miejsce jedynie w przypadkach gdy markerem nowotworowym jest enzym. Dla mostków oligonukleotydowych, hybrydyzujących z mRNA, wymagana jest już synteza konkretnego mRNA w każdej komórce. Mimo powyższych uwag wyniki pracy autorów jako badania wstępne, otwierające nową ścieżkę koncepcyjną, są na pewno wysoce wartościowe.
Literatura:
1. Photodynamic molecular beacon as an activatable photosensitizer based on protease-controlled singlet oxygen quenching and activation. Gang Zheng, Juan Chen, Klara Stefflova, Mark Jarvi, Hui Li, Brian C. Wilson. Proc. Natl. Acad. Sci. U.S.A. 104(21):8989-94, 2007.
2. Photodynamic Therapy and Photo-Imaging. Brian W. Pogue, Tayyaba Hasan. Opt. and Phot. News. 14(8):36-43, 2003.
3. Zastosowanie metody łyżeczkowania (curettage) i terapii fotodynamicznej w leczeniu raków podstawnokomókowych skóry. Aleksander Sieroń, Aleksandra Kawczyk-Krupka, Justyna Małyszek, Grzegorz Kowalski, Jacek Trompeta, Henryk Koziołek, Jacek Gawrychowski. Ann. Acad. Med. Siles. 60(4), 2006.
---
Barbara Lachowicz jest studentką biotechnologii medycznej na Uniwersytecie Wrocławskim (2003-2008). Członkini Studenckiego Koła Biotechnologów "Przybysz", działającego w obrębie macierzystej uczelni. Naukowe zainteresowania koncentrują się wokół biologii komórki - dotyczą głównie aspektu patologii/terapii nowotworów.
